در علم شیمی اصطلاحات و فرآیندهای بسیار زیادی هست که هر کدام از آنها معنی مخصوص به خود را دارند. یکی از فرآیندهای رایج و پرکاربرد در علم شیمی به خصوص در شیمی تجزیه، تیتراسیون (تیتر کردن یا تیترامتری) است که برای تعیین میزان غلظت مایعات مجهول (آنالیت) و تعیین درصد خلوص به کار گرفته میشود. از این روش ابتدا در قرن ۱۸ در فرانسه استفاده شد. روشهای متفاوتی برای انجام تیتراسیون وجود دارد که از رایجترین انواع آنها، میتوان تیتراسیون حجمسنجی اسید و باز و ردوکس را نام برد. هر چند که امروزه اکثر کارهای مرتبط با شیمی را از صفر تا صد با استفاده از دستگاههای مخصوص انجام میدهند؛ اما یادگیری و آشنا شدن با فرآیندهایی مانند تیتراسیون برای افرادی که در این حوزه مشغول به کار یا مطالعه هستند، ضروری است.
برای مثال روشهای کلاسیک برای محدوده غلظتهای پایین مناسب نیستند، و برای این غلظتها اندازهگیری با روشهای مدرن مانند آنالیز دستگاهی پیشنهاد میشود. اما در محدوده غلظتهای بالاتر، روشهای مدرن از نظر دقت دارای محدودیت هستند و استفاده از روشهای کلاسیک همچون تیتراسیون ارجحیت دارد. در این مقاله درمورد اینکه تیتراسیون چیست به طور کامل توضیح داده شده است.
فهرست مطلب
نحوه انجام تیتراسیون

تیتراسیون در واقع یک تکنیک تجزیه و تحلیل کیفی شیمیایی است که از آن برای محاسبه غلظت یک آنالیت معین در یک مخلوط استفاده میکنند. تیتراسیون یکی از مهمترین فرآیندها در حوزه شیمی تجزیه است و به دلیل اهمیت زیاد اندازهگیری حجم در تیتراسیون، گاهی اوقات از آن با نام آنالیز حجمی نیز یاد میکنند.
برای تیتراسیون باید یک تیترانت یا تیتراتور (معرف) که یک محلول استاندارد با حجم و غلظت استاندارد و از پیش تعیین شده و به صورت مایع، آماده کرد. تیترانت را میتوان به وسیله بورت به صورت قطرهای به آنالیت با غلظت نامعلوم اضافه کرد. درمورد اینکه تیتراسیون چیست باید گفت که تیترانت با آنالیت واکنش نشان خواهد داد تا زمانی که به نقطه پایانی یا هم ارزی با آن برسد. بعد از انجام این واکنش میتوان با اندازهگیری میزان تیترانت مصرفی برای رسیدن به نقطه پایانی میزان غلظت یک ماده را تعیین کرد.
در این روش معمولا میزان بسیار دقیقی از آنالیت مورد نظر را در یک فنجان یا ارلن مایر میریزند. بعد از آن مقدار بسیار کمی نشانگر مانند فنل فتالئین را در زیر یک بورت کالیبره شده یا سرنگ پیپت شیمی که از تیترانت تشکیل شده است، قرار میدهند. البته بعضی مواقع به جای استفاده از نشانگر، از pHسنج استفاده میشود.
برای اینکه بهتر متوجه شوید که تیتراسیون چیست و چگونه انجام میشود، باید گفت در تیتراسیون حجم کمی از تیترانت را به آنالیت و نشانگر اضافه میکنند. این کار را تا زمانی که نشانگر در واکنش به رسیدن آستانه اشباع تیترانت تغییر رنگ دهد، ادامه میدهند. باید حجم اضافه شده را به دقت اندازهگیری نمود و پس مشاهده اولین نشانههای واکنش، هنگامی که ماده مورد نظر تغییر رنگ میدهد، میتوان گفت که به نقطه پایانی تیتراسیون رسیدهایم. در این آزمایش میزان تیترانت مقدار آنالیت موجود در طول واکنش را متعادل میکند.
شرایط لازم برای تیتراسیون
1- تیترکننده و آنالیت حتما باید محلول باشند و اگر در ابتدا جامد هستند باید در محلول آبی حل شوند. برای حل کردن مواد جامد از حلالهایی مانند اسید استیک یا اتانول میتوان استفاده نمود. همچنین آنالیت باید حتما رقیق باشد تا دقت بیشتری داشته باشد.
2- مشخص بودن استوکیومتری واکنشها زیرا در صورت نا مشخص بودن استوکیومتری، نمیتوان از تعداد مولهای تیترانت مصرف شده در نقطه پایانی استفاده نمود و مقدار آنالیت نمونه را محاسبه کرد.
3- واکنش تیتراسیون باید با سرعت انجام شود و نباید سرعت اضافه کردن تیترانت از سرعت واکنش بین تیتر کننده و آنالیت سریعتر باشد، زیرا در این صورت نقطه پایانی از نقطه همارزی به مقدار قابل توجهی فراتر رفته و سبب خطا میشود.
4- برای تیتراسیونهای غیر اسید و باز، از یک محلول بافر در ظرف تیترانت استفاده میکنند زیرا به PH ثابت در طول واکنش تیترکردن نیاز است.
5- اگر در محلول موردنظر، علاوه بر آنالیت، واکنش دهنده دیگری نیز وجود داشته باشد، باید از محلول پوشاننده استفاده نمود تا به صورت یک پوشش برای واکنش یون ناخواسته عمل نماید.
لوازم مورد استفاده در تیتراسیون

حال که تا حدی میدانید تیتراسیون چیست، باید گفت که تجهیزات مورد نیاز بسته به نوع تیتراسیون میتواند متفاوت باشد. برای مثال برخی از تیتراسیونها ممکن است که به لوازمی مانند بورتها و پیپتها نیاز داشته باشند. در حالی که مدلهای دیگر تیتراسیون ممکن است که به تجهیزاتی مانند فلاسکهای حجمی و همزن نیاز داشته باشند. برخی از تیتراسیونهای خاص نیز هستند که تنها با تجهیزات مخصوص آزمایشگاهی قابل انجامند. به طور کلی برخی از وسایلی متداولی که برای تیتراسیون نیاز خواهد داشت، شامل وسایل زیر است:
- ارلن مایر
- بالن ژوژه
- بشر
- پوآر
- بالن
- ترازو
- استوانه مدرج
- قیف
- تیتراتور خودکار
- کارل فیشر تیتراتور
- تیتراتور پتانسیومتری
- تیتراتور دماسنج
حال که متوجه شدید تیتراسیون چیست، باید این را هم بدانید که برای خرید تجهیزات مرتبط با این فرآیند باید دقت زیادی داشته باشید؛ چرا که تیتراسیونهای مختلف به وسایل متفاوت نیاز دارند.
انواع تیتراسیون

تیتراسیون انواع مختلفی دارد که باتوجه به نوع آنالیت مورد استفاده قرار میگیرند مانند تیتراسیون اسید/بازی، معکوس یا برگشتی، ردوکس، بارش، مستقیم، غیرمستقیم یا جایگزینی، وزنی، رسوبی، تیتراسیون سنجش، یدومتری، کارل فیشر، پتانسیومتری، کمپلکسومتری و غیره دارد که هر کدام به وسایل مخصوص نیاز دارند.
تیتراسیون اسید/بازی: دراین روش یک تیترانت از جنس باز یا اسید با آنالیتی که آن هم باز یا اسید است درگیر واکنش میشود و در واقع این واکنش، واکنش خنثی شدن اسید و باز است.
تیتراسیون برگشتی: از این روش در مواردی که نمیتوان از تیتراسیون مستقیم استفاده کرد و نقطه اکیوالان یا همارزی نامشخص است، استفاده میشود. در این روش غلظت آنالیت به صورت غیر مستقیم تعیین میشود.
تیتراسیون ردوکس: این روش بر مبنای واکنشهای اکسایش-کاهش میباشد و در آن تیترانت یک ماده اکسید کننده یا کاهش دهنده است. معمولا در این فرایند نیازی به استفاده از نشانگر نیست زیرا واکنش دهندهها رنگی هستند.
تیتراسیون بارش: این روش با تشکیل یک رسوب نامحلول هنگامی که دو ماده واکنش دهنده باهم تماس پیدا میکنند، اتفاق میافتد. مثلا وقتی که محلول نیترات نقره با محلول تیوسیانات آمونیوم یا محلول کلرید سدیم واکنش میدهد، رسوب سفیدی از کلرید نقره یا تیوسیانات نقره را تشکیل میدهد.
تیتراسیون کمپلکسومتری: این تیتراسیون به واکنش کمپلکس شدن یک فلز با یک لیگاند گفته میشود. و معمولا از معرف دیسدیم اتیلن دیآمین تترا استات در این واکنش استفاده میشود.
تیتراسیون رسوبی: از این روش برای تعیین غلظت عناصر استفاده میشود و در نهایت محصول این واکنش رسوب خواهد کرد. در این تیتراسیون از تیترانتهای غیرآلی و تیتراسیونهای سورفكتنتها استفاده میشود.
تیتراسیون یدومتری: در این واکنش ید نقش نشانگر را دارد و اکسید میشود و تیترانت آن معمولا تیوسولفات است.
تیتراسیون مستقیم: این روش تیترسنجی یک روش پایه است که در آن بین ترکیب ناشناخته و ترکیب با غلظت مشخص واکنش رخ میدهد. در این روش ترکیب ناشناخته با ترکیب شناخته شده مستقیما واکنش میدهد و از معرفهای اضافه استفاده نمیشود.
تیتراسیون غیرمستقیم یا جایگزینی: در این روش نمونه مورد بررسی نامحلول و ناپایدار است، و به همین دلیل آنالیت با مادهای دیگر واکنش میدهد. به این معنی که آنالیت به طور مستقیم در فرآیند تیتراسیون شرکت نخواهد کرد و یا رسوب میکند یا از محلول خارج میشود. در اینجا، مقدار مولهای ماده جایگزین محاسبه و به مقدار انالیت مورد نظر ربط داده میشود.
یکیدیگر از انواع تیتراسیون تیتراسیون فاز گاز است. این دسته از تیتراسیونهایی هستند که در فاز گاز انجام میشوند. از این تیتراسیون برای تعیین گونههای فعال از طریق واکنش با مقداری گاز دیگر به عنوان تیترانت استفاده میشود.
اصطلاحات رایج در تیتراسیون
آنالیت: به محلولی با غلظت یا درصد خلوص نامشخص گفته میشود.
تیترانت: نامهای دیگری مثل معرف، تیتراتور دارد و به محلولی استاندارد با حجم و غلظت و فرمول شیمیایی مشخص و استاندارد گفته میشود که برای تعیین غلظت یا درصد خلوص آنالیت استفاده میشود.
نشانگر (شناساگر): مادهای رنگی است که هنگامی که واکنش پایان مییابد تغییر رنگ میدهد و معمولا از جنس اسید یا باز ضعیف است.
-
تیتراسیون آنالیز وزنی
این اصطلاح برای عناصری به کار برده میشود که میتوانند نمکهای نامحلول را در محلول آبی تشکیل دهند. در این فرآیند جداسازی یونها از ترکیب به شکل رسوب انجام میشود. برای انجام این فرآیند کافی است که طبق مراحل زیر پیش بروید:
- نمونه را به مقدار مشخصی آماده کنید.
- جزء مورد نیاز در نمونه را، به رسوب تبدیل کنید.
- رسوب را خالص کنید و مورد آزمایش قرار دهید که به کمک آن غلظت یا خلوص نمونه به دست میآید.
- نقطه همارزی یا نقطه اکیوالان را مشخص کنید.
اگر در قسمتهای قبلی مقاله برایتان سوال پیش آمده است که نقطه هم ارزی تیتراسیون چیست، در اینجا به سوال شما جواب داده شده است. نقطه هم ارزی در واقع نقطهای در واکنش است که در آن تعداد معادلهای تیترانت و آنالیت برابر میشوند و در این نقطه مقدار کافی از نیترات مصرف شده است.
نقطه پایانی: نقطه پایانی، نشان دهنده پایان تیتراسیون است. در این نقطه تیترانت به قدری اضافه شده است که تعداد مول تیترانت با تعداد مول آنالیت برابر شده است. برای اینکه بهتر درک کنید تیتراسیون چیست و نقطه پایانی در آن چه نقشی دارد، به این مثال توجه کنید. فنل فتالئین یا متیل اورانژ را میتوان برای تیتراسیون اسیدها و بازها استفاده کرد. اندیکاتورها با تغییر رنگ خود میتوانند نقطه پایانی را نشان دهند. گاهی اوقات یکی از واکنش دهندهها نیز میتواند به عنوان یک نشانگر عمل کند.
تفاوت نقطه همارزی با نقطه پایانی: نقطه همارزی از روی نمودار سنجش حجمی تعیین میشود. در حین آزمایش، با مشاهده اولین تغییر رنگ در محلول، میتوان به نقطه همارزی پی برد. نقطه پایانی و نقطه همارزی فاصله کمی از هم دارند. رسیدن به نقطه پایانی زمانی مشخص میشود که تغییر رنگ در محلول ثابت بماند.
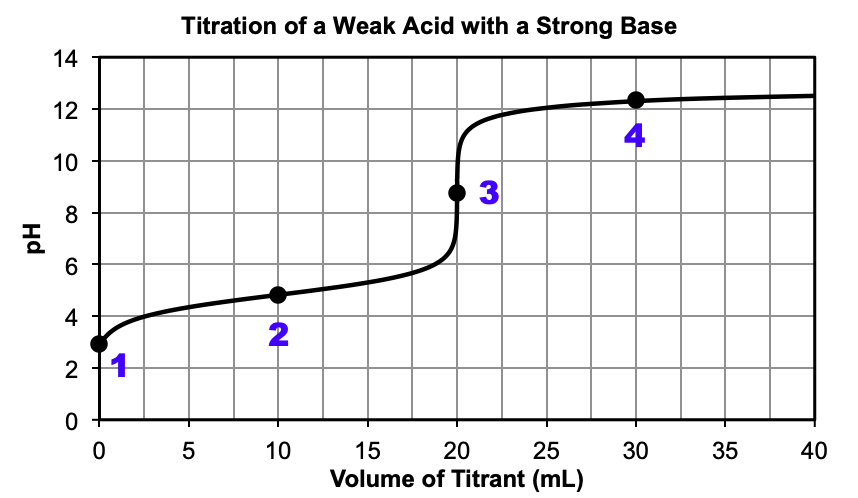
منحنی تیتراسیون: این منحنی یک محور افقی (x ) دارد که نشان دهنده حجم نیترانتی است که از ابتدای واکنش اضافه شده و یک محور عمود (y) نیز دارد که نشان دهنده غلظت آنالیت در آن حجم است. اگر در فرآیند تیترکردن از اسید و باز قوی استفاده شود، تغییرات pH بر روی محور y قرار میگیرد. در این حالت، یک شیب تند در نقطه همارزی مشاهده میشود و تغییرات کم در طول نمودار ایجاد میگردد.
محاسبات تیتراسیون
برای محاسبات تیتراسیون یک فرمول و قانون کلی هست که به شرح زیر است:
Ca = CtVt M / Va
در این فرمول Ca غلظت آنالیت، Ct غلظت تیترانت، Vt حجم تیترانت، M نسبت مولار واکنش دهندگان تیتراسیون و Va حجم آنالیت است. این رابطه بر اساس استیوکیومتری واکنش بین تیترانت و آنالیت به دست میآید و میتوان به کمک آن غلظت مادههای مورد نظر را به دست آورد. همچنین تمامی جدولهای در واکنش تیتراسیون بر اساس این فرمول رسم میشوند.
همچنین در هنگام انجام تیتراسیون ممکن است خطایی رخ دهد. مهمترین منشا خطا در تیتراسیون اسید-باز، تعیین کردن نقطه پایانی است. ممکن است یک قطره تیترانت کم یا زیاد ریخته شود و محاسبات را دچار مشکل کند. برای محاسبه خطای تیتراسیون از معادله هاندرسون هاسلباخ استفاده میشود. اگر غلظت به دست آمده در واقعیت، با غلظت به دست آمده از فرمول یکی نباشد، خطای تیتراسیون مشخص میشود. در هنگام رسم نمودار تیتراسیون، pH محلول آنالیت در مقابل حجم تیترانت قرار داده میشود.
کاربردهای تیتراسیون
جالب است بدانیم فرایند تیتراسیون علاوه بر تعیین غلظت، کاربردهای دیگری نیز دارد که در زیر به شرح چند نمونه از این کاربردها خواهیم پرداخت:
1- تعیین اسیدیته و قلیائیت نمونه آب
2- تعیین سختی آب
3- تعیین نیتروژن کل به روش کجلدال
4- استفاده به عنوان روشهای حجمسنجی در صنایع مختلف مانند صنایع غذایی، آب و فاضلاب، معدن، داروسازی و …
5- تهیه سوختهای زیستی با استفاده از تیتراسیون اسید و باز
6- تعیین اکسیژن در آب با استفاده از تیتراسیون ردوکس
7- معرف بندیگ و تعیین گلوکز اضافه در ادرار
8- استفاده در آزمایشگاههای تشخیص طبی، آزمایشگاههای شیمی
9- تعیین غلظت ویروسها و باکتریها در علم زیست شناسی
نتیجهگیری
در شیمی اصطلاحات و فرآیندهای زیادی وجود دارند که برای برخی از افراد ممکن است نامفهوم باشند. یکی از فرآیندهایی که در شیمی تجزیه اهمیت بسیار زیادی دارد، تیتراسیون است. تیتراسیون یک روش آزمایشگاهی معمول کمی در شیمی تجزیه است که برای تعیین غلظت یک محلول مجهول با روشهای مختلف به کار می رود. برای اینکه بهتر بدانید تیتراسیون چیست، در این مقاله درمورد تیتراسیون، تجهیزات مورد نیاز آن، اصطلاحات رایج در آن، نحوه انجام تیتراسیون و محاسبات مرتبط با آن توضیح داده شد.