اسید اگزالیک یک ترکیب بیرنگ، کریستالی و آلی از خانواده دیکربوکسیلیک اسید است و در بسیاری از گیاهان پیدا میشود. این ماده در صنایع مختلفی مانند نساجی، پزشکی، شیمیایی، مواد معدنی و ... استفاده میشود. ما در این مقاله توضیح میدهیم که اسید اگزالیک چیست و چه کاربردهایی دارد. همچنین به روش تولید این ماده و نحوه نگهداری و ایمنی آن اشاره میکنیم.
فهرست مطلب
مشخصات شیمیایی و فیزیکی اسید اگزالیک
اسید اگزالیک (Oxalic acid) ساختاری با دو پلیمر دارد و به حالت جامد و سفید کریستالی موجود است. این ماده در آب قابل حل است و در هنگام حل شدن در آب به صورت یک مایع بدون رنگ در میآید. این ماده یک عامل کاهنده با فرمول C2H2O4 است. اسید اگزالیک در شیره سلولی گونههای اگزالیس و رومکس گیاهان به صورت نمک پتاسیم و کلسیم موجود است. اسید اگزالیک در یک محلول آبی تبدیل به یک اسید ضعیف میشود که یونیزه میشود. اسید اگزالیک یکی از پر قدرتترین اسیدهای طبیعی است. این اسید در پاک کنندههای سطوح، زنبورداری، رنگرزی و تولید ضدیخ کاربرد دارد.
| فرمول مولکولی | C۲H۲O۴ |
| جرم مولی | 90.03 g mol−1 (anhydrous) 126.07 g mol-1 (dihydrate) |
| شکل ظاهری | کریستال سفید |
| دمای ذوب | 189 to 191 °C (372 to 376 °F; 462 to 464 K) 101.5 °C (214.7 °F; 374.6 K) dihydrate |
| چگالی | 1.90 g cm-3 (anhydrous) 1.653 g cm-3 (dihydrate) |
| انحلال پذیری در آب | 14.3 g/100ml (25 °C) |
| انحلال پذیری |
23.7 g/100ml (15 °C) in اتانول 1.4 g/100ml (15 °C) in دیاتیل اتر |
اسفناج، کلم، کلم بروکلی و ... سرشار از اگزالات و اسید اگزالیک هستند. اسید اگزالیک قطبی است و در همه حلالهای قطبی حل میشود. گریدهای اسید اگزالیک عبارتند از: گرید خالص (purified grade)، گرید آزمایشگاهی، گرید تکنیکال، گرید صنعتی، گرید دارویی، گرید معرف، گرید خوراکی و گرید AR.
نحوه تولید و روشهای تولید اسید اگزالیک
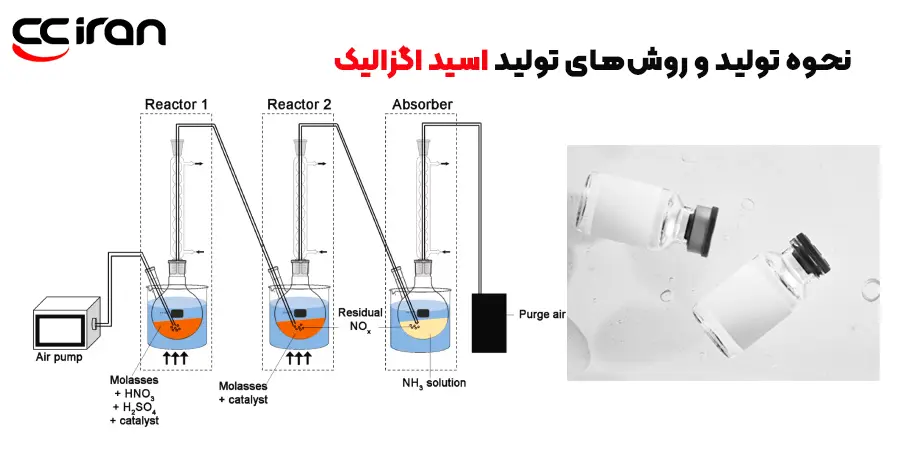
اولین بار اگزالیک اسید در سال 1745 از خاکشیر استخراج شد. بعدها آن را از واکنش بین شکر و اسید نیتریک غلیظ تهیه کردند و در 1824 یک دانشمند آلمانی این ماده را از واکنش سیانوژن با محلول آبی آمونیاک تهیه کرد. برای درک بهتر از اینکه اسید اگزالیک چیست، لازم است با روشهای تولید این ماده آشنا شوید. به راحتی میشود اسید اگزالیک را با اکسیداسیون کربوهیدراتها مانند ساکارز یا غلیظ کردن اسید نیتریک به وجود آورد. برای تهیه اسید اگزالیک بهتر است مراحل زیر را دنبال کنید:
- 10 گرم نیشکر را در یک ارلن 250 میلیلیتری بریزید.
- 50 میلیلیتر اسید نیتریک غلیظ را اضافه کنید و آن را بر روی یک حمام آب جوش یا بنماری قرار دهید.
- مخلوط گرم میشود و بیشتر شکر موجود در ظرف حل میشود.
- ارلن را بردارید و در چوبی آن را بگذارید. بعد از 15 دقیقه محلول داغ را در ظرف تبخیر بریزید و ارلن را با 10 میلیگرم اسید نیتریک غلیظ بشویید و آن را به ظرف تبخیر اضافه کنید.
- اجازه دهید محلول تبخیر شود تا حجم آن به 10 میلیلیتر برسد.
- محلول را در مخلوط آب یخ خنک کنید تا اسید اگزالیک متبلور شود.
- محلول را روی قیف بوخنر بریزید تا اسید اگزالیک باقی بماند.
- محصول را با کاغذ صافی خشک کنید و سپس آن را در هوای آزاد قرار دهید.
- در پایان حدود 3.5 گرم اسید اگزالیک به دست میآید.
روش دیگر برای تهیه این ماده تهیه دیاستر از طریق واکنش کربونیلاسیون الکلها و در ادامه هیدرولیز دی استر به اگزالیم اسید است.
4 ROH + 4 CO + O2 → 2 (CO2R)2 + 2 H2O
کاربرد اسید اگزالیک در صنایع مختلف

-
از بین بردن لکها و زنگ
این ماده قدرت تمیز کنندگی بسیار بالایی دارد و انواع لکها را از سطوح پاک میکند. این اسید را میتوان برای از بین بردن زنگ زدگی فلزات استفاده کرد. همچنین در صنعت نساجی برای سفید کردن لباسها استفاده میشود.
-
مصارف صنعتی
این ماده شیمیایی در فراوری مواد معدنی و استریل کردن تجهیزات به کار میرود. همچنین اسید اگزالیک در فرایند رنگرزی نقش ماده خشک کننده را دارد.
-
صنعت پزشکی و دارویی
اسید اگزالیک برای تصفیه یا رقیق کردن مواد شیمیایی به کار برده میشود. البته این ماده ممکن است در بعضی موارد برای بدن ضرر داشته باشد. صنعت داروسازی از اسید اگزالیک در فرمولاسیونهای دارویی خاصی استفاده میکند که در آن به عنوان یک عامل کاهنده یا عامل کیلیت عمل میکند.
-
صنعت زنبورداری
اسید اگزالیک در صنعت زنبورداری برای مقابله کنه واروا استفاده میشود.
-
صنعت آب و فاضلاب
این ماده در تصفیه خانههای فاضلاب استفاده میشود تا آهک به طور کامل از آب حذف شود.
-
صنعت عکاسی
این ماده یک عامل کاهنده در تولید فیلمهای عکاسی است. توانایی آن در سفید کردن و رنگ آمیزی پرینتهای عکاسی آن را به ابزاری ارزشمند برای افزایش کیفیت تصویر تبدیل کرده است. اینبخش به بررسی نقاط عطف تاریخی و تکنیکهای مربوط به استفاده از اسید اگزالیک در اتاق تاریک میپردازد. رنگ آمیزی تصویر یک تکنیک هنری است که برای افزودن رنگهای ظریف و زیبایی شناختی به عکسها استفاده میشود. اسید اگزالیک با سفید کردن و رنگ کردن انتخابی تصویر، نقش مهمی در این فرآیند ایفا میکند و در نتیجه جلوههای بصری منحصربهفردی ایجاد میکند.
-
صنایع شیمیایی
باید اشاره کنیم که اسید اگزالیک برای لانتانیدها یک معرف بسیار مهم است. اگزالاتهای لانتانید هیدراته در محلولهای بسیار اسیدی فیلتر میشوند و کریستالهای غیر لانتانیدی به وجود میآورند.
-
سفید کردن چوب
در صنعت نجاری، اسید اگزالیک معمولاً برای اهداف سفید کردن چوب استفاده میشود. با از بین بردن لکههای ناشی از واترمارک یا سایر تغییر رنگها، رنگ چوب را روشن میکند.
-
در صنعت پلاستیک
در پلاستیکهای pv، پلاستیکهای آمین، پلاستیکهای اوره و در محلول استون در واکنش رزین اپوکسین به عنوان کاتالیزور عمل میکند. این ترکیب درسنتز مواد آلی مثل کبالت اگزالات، نیکل اگزالات، کالیک اسید، هیدروکسینون و پنتا اریتریتول هم کاربردهایی دارد.
کاربردهای دیگر اسید اگزالیک
- کاهنده در واکنشهای شیمیایی
- آفتکش کشاورزی
- حذف یون کلسیم
- در تهیه ضدیخها
- به عنوان معرف در آنالیز دستگاهی سیلیس
- برای تولید گلوکز از نشاسته
- به عنوان ضد انعقاد خون در نمونههای خون
- در صنعت لاستیک (پاک کردن چرخ خودرو)
- به عنوان اسید شستشو در خشکشوییها
- جهت تصفیه متانول
- در مواد شیمیایی حساس به نور
- عامل آبکاری و اصلاح سطح و پوشش
- صنعت رنگرزی به عنوان تثبیت کننده رنگ
شرایط ایمنی و نگهداری اسید اگزالیک

احتمالا برایتان سوال پیش آمده باشد که شرایط ایمنی اسید اگزالیک چیست. باید اشاره کنیم که اسید اگزالیک یک سم قوی است و در صورت استعمال بیش از حد باعث از بین رفتن قلب و عروق و مرگ میشود. در صورت مسموم شدن با اسید اگزالیک دچار علائمی مانند استفراغ، اسهال، آسیبهای کلیوی، شوک، تشنج و حتی کما میشوید. حتی استنشاق این ماده هم به کلیه آسیب میرساند؛ زیرا اگزالات در کلیه رسوب میکند و به آن آسیب میزند. همچنین تماس با این ماده منجر به بثورات پوستی، قرمزی، تاول و زخم میشود. اگر این ماده به اشتباه بلعیده شود، به سرعت به نزدیکترین بیمارستان مراجعه کنید.
لازم است در هنگام کار با این ماده از دستکش لاتکس، عینک محافظ و ماسک گاز استفاده کنید. اسید اگزالیک را در یک مکان با تهویه مناسب و به دور از مناطق مسکونی نگهداری کنید. این ماده باید در یک محیط خشک و به دور از دیگر مواد نگهداری شود. محلول این ماده تا یک هفته در دمای اتاق باقی میماند و در صورت نگهداری در یخچال، حدود چند ماه دوام دارد. اگر محلول تغییر رنگ داد یا بوی به خصوصی داد، آن را به سرعت دور بریزید. این ماده باید از نقره، کلرید و اوره دور نگه داشته شود زیرا با این مواد ناسازگار میباشد. در کل به دلیل داشتن خاصیت اسیدی باید از قلیا و محیطهای قلیایی به دور باشد و در مجاورت بازها و فلزات فعالی نظیر سدیم، پتاسیم و منیزیم قرار نگیرد. از نگهداری این ترکیب در مجاورت موادی که با این ترکیب گاز سمی تولید میکنند، مانند سدیم سیانید و سولفید آهن اجتناب کنید. از نگهداری جامدات یا اسیدهای اکسید کننده در مجاورت این اسید خودداری کنید.
سوالات متداول
-
اثرات این ماده بر بدن انسان چیست؟
مصرف زیاد مواد غذایی حاوی اسید اگزالیک منجر به ایجاد سنگ کلیه میشود. به علت خاصیت کیلیت کنندگیای که دارد از جذب کلسیم و آهن جلوگیری میکند. در صورت مصرف بالای مواد غذایی حاوی آن میتواند منجر به فقر آهن و مشکلات استخوان شود.
نتیجهگیری
اسید اگزالیک یک نوع دیکربوکسیلیک اسید است، به صورت یک ترکیب طبیعی در گیاهان و سبزیجات یافت میشود، سادهترین دیکربوکسیلیک اسید است و قدرت اسیدی آن بیشتر از اسید استیک است. این ماده هم از اکسیداسیون کربوهیدراتها و هم در آزمایشگاهها با اکسیداسیون ساکارز در حضور اسید نیتریک و با یک کاتالیزور مانند پنتا اکسید وانادیوم تولید میشود. ما در این مقاله توضیح دادیم که اسید اگزالیک چیست، کاربردهای آن در چه صنایعی است و شرایط ایمنی و نگهداری این ماده چگونه است.