اگر به زندگی روزمره خود نگاهی بیندازید، رد پای علم شیمی را در ابعاد مختلف آن مشاهده خواهید کرد. در این مقاله قصد داریم به بررسی کاربرد و اهمیت اسید فرمیک و اسید اگزالیک در صنعت زنبورداری بپردازیم. اسید فرمیک را اغلب در نیش حشراتی مانند زنبور و مورچه پیدا خواهید کرد. نام آن نیز از کلمه لاتین formica به معنای مورچه گرفته شده که به تقطیر بدن مورچه و جداسازی این اسید اشاره میکند. مورد بعدی که اسید اگزالیک نام دارد که در سبزیجات مختلف یافت شده و به وسیله اکسیداسیون کربوهیدراتها در دو شکل مختلف تولید خواهد شد. برای اطلاعات بیشتر درمورد کاربرد و اهمیت اسید فرمیک و اسید اگزالیک در صنعت زنبورداری، ادامه مقاله را بخوانید.
فهرست مطلب
- خواص فرمیک اسید
- انواع اسید فرمیک
- کاربردهای اسید فرمیک
- عوارض و خطرات اسید فرمیک
- شرایط نگهداری و موارد ایمنی اسید فرمیک
- خواص اسید اگزالیک
- روش تولید اسید اگزالیک
- کاربرد اسید اگزالیک
- عوارض و خطرات اسید اگزالیک
- نکات ایمنی نگهداری اسید اگزالیک
- دلیل و نحوه استفاده از اسید فرمیک و اسید اگزالیک در صنعت زنبورداری
- سیکل زمانی استفاده از این محصول در زنبورداری
- سوالات متداول
- نتیجهگیری
خواص فرمیک اسید

اسید فرمیک (Formic acid) به راحتی با آب و بیشتر حلالهای آلی قطبی مخلوط میشود. در هیدروکربنها هم تا حدی حل میشود. این ماده به صورت یک شبکه متشکل از مولکولهای اسید فرمیک با پیوند هیدروژنی تشکیل شده است. خصوصیات شیمیایی فرمیک اسید شبیه به باقی اسیدهای کربوکسیلیک است. از آن جایی که این ماده برخی از خواصهای کاهنده آلدهیدها را دارد، در نتیجه گرما ممکن است موجب تجزیه اسید فرمیک به مونوکسید کربن و آب شود. نکته منحصر به فرد آن در میان اسیدهای کربوکسیلیک این است که قادر به شرکت در واکنشهای افزودن با آلکنها خواهد بود. در نهایت اسید فرمیک و آلکنها به سادگی واکنش داده و استرهای فرمت به وجود میآیند. یکی دیگر از ویژگیهای اسید فرمیک واکنش آن با اسیدهای قوی و آلومینیوم است. اگر این اسید در تماس با الکلها و اکسیدکنندههای قوی قرار بگیرد باعث انفجار میشود.
| نام آیوپاک | متانوئیک اسید |
| نام متداول | اسید فرمیک- جوهر مورچه |
| شکل ظاهری | مایعی بی رنگ |
| فرمول مولکولی | CH2O۲ |
| جرم مولی | 46.03 g/mol |
| چگالی | 1.22 g/mL |
| دمای ذوب | 8.3 °C |
| دمای جوش | 100.8 °C |
| ثابت تفکیک اسیدی (pka) | 3.75 |
| گرانروی در دمای 26 درجه سانتی گراد | 1.57cP |
یکی از روشهای تولید آن به این صورت است که متانول و مونوکسید کربن در حضور یک باز قوی مانند مونوکسید سدیم در فشار ۴۰ اتمسفر واکنش میدهند و متیل فرمات تولید میشود. سپس از آبکافت یا هیدرولیز متیل فرمات، اسید فرمیک ایجاد میشود. به استر، نمک و آنیون حاصل از اسید فرمیک، فرمات گفته میشود.
انواع اسید فرمیک

اسید فرمیک به سه دسته کلی تقسیم میشود که هر کدام کاربرد مختص به خود را دارند.
اسید فرمیک گازی: این دسته از اسید فرمیکها، به صورت دیمر میباشد که دارای پیوندهای هیدروژنی هستند.
اسید فرمیک مایع: این دسته از مواد دارای مولکولهای نامحدود با پیوندهای هیدروژنی هستند.
اسید فرمیک جامد: این دسته از اسید فرمیکها نیز مانند اسید فرمیکهای مایع، در ساختار خود مولکولهای نامحدود با پیوندهای هیدروژنی دارند.
کاربردهای اسید فرمیک

کاربردهای اسید فرمیک به شرح ذیل میباشد:
- در درمان بیماری زگیل
- به عنوان پیل سوختی
- تولید مونوکسید کربن
- در الکتروفورز مویرگی
- منبعی برای گروه فرمیل
- تقویت تخمیر اسید لاکتیک
- در تولید عطرهای مصنوعی
- به عنوان منبع یون هیدرید
- سرکوب تشکیل اسید بوتیریک
- در استرهای فرمت طعم دهندهها
- به عنوان یک اصلاحکننده فرار pH
- تعویق پوسیدگی مواد غذایی دام
- به عنوان وسیلهای برای ذخیره هیدروژن
- استفاده در صنعت چرم سازی و دباغی
- در زنبور داری به عنوان کشنده در برابر کنه
- در صنعت نساجی در بخش رنگ کردن پارچهها
- خواص نگهدارنده و آنتی باکتریال در خوراک دام
- به عنوان یک ماده منعقد کننده در تولید لاستیک
- به عنوان منبع هیدروژن در انتقال هیدروژناسیون
- کاهش از دست دادن ارزش غذایی در فرآیند تخمیر
- استفاده در بخش دارویی و درمانی در ساخت انسولین و کافئین
- به عنوان فاز متحرک در در کروماتوگرافی مایع با عملکرد بالا HPLC
- به عنوان واسطه برای تولید ایزوبوتانول از CO2 با استفاده از میکروبها
- به جای اسیدهای معدنی برای محصولات تمیزکننده مختلف مانند پاک کننده آهک
عوارض و خطرات اسید فرمیک
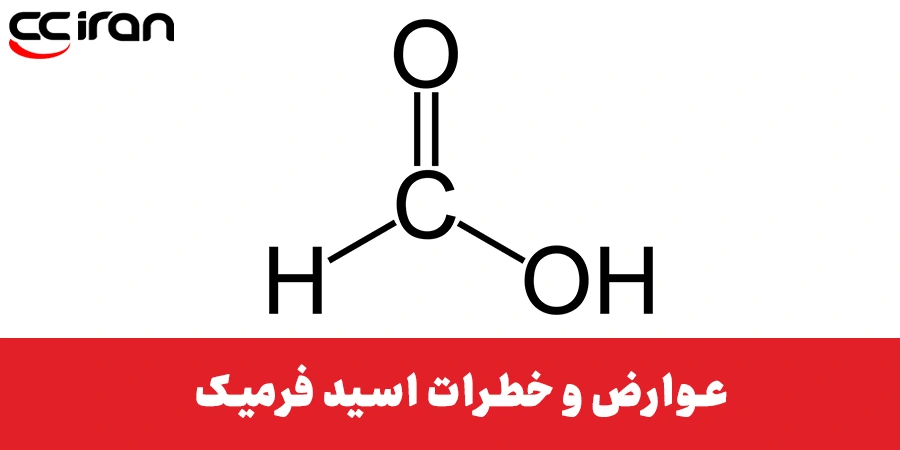
اسید فرمیک برای سلامت انسان به شدت مضر است. در صورت تماس مستقیم با پوست و چشم، سریعا آن را با آب فراوان بشویید. حالت مایع این ماده باعث آسیب جدی به قرنیه، التهاب شدید، سوختگی و کوری میشود. و در صورت تماس با پوست باعث سوختگیهای شدید همراه با قرمزی، جراحات پوستی و ترک خوردگی میشود. در صورت تماس با چشم حتماً به پزشک مراجعه کنید. در صورت استنشاق اسید فرمیک، امکان مسمویت وجود دارد سریعا به هوای آزاد بروید. استنشاق این ماده باعث تحریک سیستم تنفسی میشود که با تخریب سلولهای بویایی و سرفه همراه است. در صورتی که اسید فرمیک بلعیده شد، دهان خود را بشویید. اسید فرمیک مادهای مضر است و باعث تخریب بافتهای بدن و آسیب جدی میشود این ماده باعث سوختگی و سوراخ شدن دستگاه گوارش میشود. به وجود آمدن مشکلاتی مانند: اسهال خونی، احساس سوزش، افزایش ضربان نبض، مشکل تنفسی، صدمه به کلیه و در نهایت مرگ از عوارض جدی بلعیدن اسید فرمیک است، که البته همهی این موارد در دوزهای بالای 30ml قابل مشاهده است. در صورت نشت اسید فرمیک، از جاذبهای جامد مانند خاک کمک بگیرید. در صورت هر گونه تماس با این ماده به پزشک مراجعه کنید.
شرایط نگهداری و موارد ایمنی اسید فرمیک
اسید فرمیک باید در محیط خشک و خنک نگهداری شود چون اسید فرمیک به رطوبت و گرما حساس است و در کنار کربن دیاکسید و آب احتمال تجزیه آن وجود دارد، که به خاطر این موضوع باعث ایجاد گازهای تحریک کننده و بخارات قابل اشتعال میشود. اسید فرمیک را فقط در زیر هود مخصوص بخارات مواد شیمیایی استفاده کنید. این ماده باید به دور از منابع اشتعال نگهداری شود. ظروف نگهداری اسید فرمیک را به صورت کاملاً بسته نگهداری کنید. بهتر است برای غلبه کردن بر تجمع فشار بخار، ظروف نگهداری اسید فرمیک را به شکل دورهای تخلیه کنید. اسید فرمیک را بر روی سطوح مختلف اسپری نکنید. هنگام کار کردن با اسید فرمیک حتماً از لباسهای مخصوص و ماسکهای محافظ صورت استفاده کنید.
خواص اسید اگزالیک
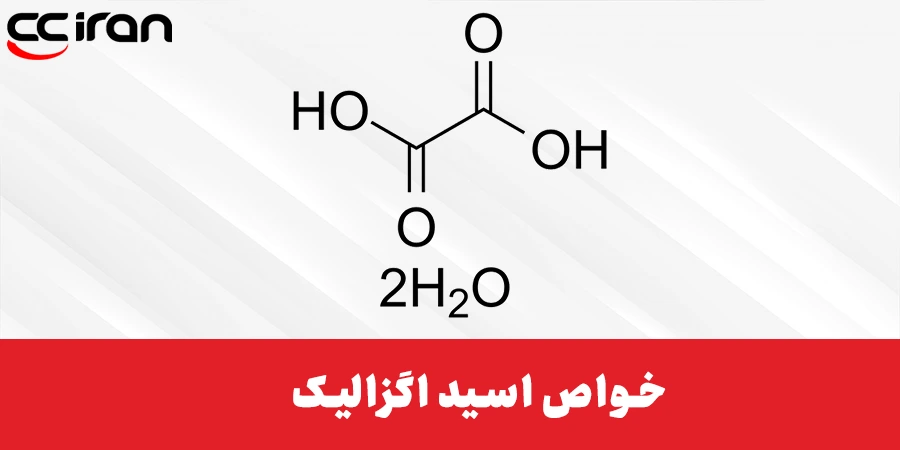
همانطور که گفتیم، سادهترین نوع اسید اگزالیک (Oxalic acid) در سبزیجات و گیاهان، با فرمول HOOC-COOH یافت میشود که قدرت اسیدی بالاتری نسبت به اسید استیک دارد. به همین دلیل استفاده بیش از اندازه آن خطرناک و آسیب زننده خواهد بود. این ماده ساختاری با دو پلی مورف دارد و به شکل جامد کریستالی سفید رنگ موجود است، اما به محض حل شدن در آب، به یک محلول بیرنگ تبدیل خواهد شد.
از آنجایی که نحوه تهیه اسید اگزالیک بسیار ساده است، کاربرد آن نیز گستره خواهد بود. برای تهیه این اسید، لازم است به اکسیداسیون کربوهیدراتهای مشخصی مانند ساکارز با اسید نیتریک بپردازید. در طی اکسیداسیون، اتمهای کربن به صورت جفت تقسیم شده و در نهایت اسید اگزالیک به وجود میآید. از کابردهای پر اهمیت آن نیز میتوان به فرآیند رنگرزی به عنوان ماده رنگزا، شیمی لانتانید به عنوان یک معرف، درخشندگی مجسمههای مرمر و غیره اشاره کرد. در ادامه کاربرد و اهمیت اسید فرمیک و اسید اگزالیک در صنعت زنبورداری که یکی از مهمترین کاربردها است، بررسی خواهیم کرد.
| فرمول مولکولی | C۲H۲O۴ |
| شکل ظاهری | جامد کریستالی سفید بیرنگ |
| جرم مولی |
90.03 g mol−1 (anhydrous) 126.07 (g mol-1 (dihydrate |
| چگالی |
1.90 g cm-3 (anhydrous) 1.653 g cm-3 (dihydrate) |
| انحلال پذیری در آب | 14.3 g/100ml (25 °C) |
| انحلال پذیری |
23.7 g/100ml (15 °C) in اتانول 1.4 g/100ml (15 °C) in دیاتیل اتر |
روش تولید اسید اگزالیک

اسید اگزالیک از واکنش اکسیداسیون کربوهیدراتها و یا گلوکز با استفاده از اسید نیتریک و یا هوا در حضور کاتالیزور وانادیم پنتا اکسید میتوان سنتز کرد. همچنین روش دیگر برای تهیه این ماده تهیه دیاستر از طریق واکنش کربونیلاسیون الکلها و در ادامه هیدرولیز دی استر به اگزالیم اسید است.
4 ROH + 4 CO + O2 → 2 (CO2R)2 + 2 H2O
کاربرد اسید اگزالیک
- حذف یون کلسیم
- در تهیه ضد یخها
- جهت تصفیه متانول
- فعال کننده سطح
- در صنعت زنبورداری
- برای تصفیه فاضلاب
- در لوازم عکاسی، فیلم
- برای تولید گلوکز از نشاسته
- کاهنده در واکنشهای شیمیایی
- در مواد شیمیایی حساس به نور
- عامل آبکاری و اصلاح سطح و پوشش
- حلال در برخی از واکنشهای شیمیایی
- عامل پاککننده (ازبین بردن زنگزدگی)
- در صنعت لاستیک (پاککردن چرخ خودرو)
- صنعت رنگرزی به عنوان تثبیت کننده رنگ
- بهعنوان معرف در آنالیز دستگاهی سیلیس
- بهعنوان اسید شستشو در خشکشوییها
- بهعنوان ضد انعقاد خون در نمونههای خون
عوارض و خطرات اسید اگزالیک
این اسید در حالت خالص اشتعال پذیر است و در صورتی که در محیط گرم یا نزدیک حرارت باشد آتش میگیرد. در دسته ترکیبات خورنده قرار دارد.
در صورت تماس چشمی: تا دریافت کمکهای پزشکی چشمها را با آب فراوان به مدت 15 دقیقه شستشو دهید، مطمئن شوید آب شستشو به راحتی از چشم خارج میشود.
در صورت تماس با پوست: در تماس با پوست میتوان گفت ممکن است سبب ایجاد تورم، قرمزی و حتی سوختگی نماید. پس لازم است محل تماس را با آب زیاد شستشو داده و مطمئن شوید ماده به طور کامل از روی پوست برداشته شده است. با این حال در صورت بروز هرگونه عوامل دیگر به پزشک مراجعه کنید. حتما قبل از استفاده مجدد از کفش، لباس و تجهیزات آنها را بشویید.
در صورت بلعیدن: در صورتی که مصدوم هوشیاری دارد لازم است تا دریافت کمکهای پزشکی یک لیوان آب به او بنوشانید، در صورتی که مصدوم هوشیاری نداشت چیزی به مصدوم نخورانید.
در صورت استنشاق: استنشاق این ماده باعث سوزش مجاری تنفسی میگردد بنابراین لازم است مصدوم را به هوای آزاد برسانید تا روند تنفس وی عادی شود، در صورت نیاز و بروز هرگونه علائم دیگر به پزشک مراجعه کنید.
نکات ایمنی نگهداری اسید اگزالیک
اسید اگزالیک را باید در ظروف کاملا سربسته و در محل خشک و خنک نگهداری کرد. در کل به دلیل داشتن خاصیت اسیدی باید از قلیا و محیطهای قلیایی کاملا به دور باشد و در کنار بازها و فلزات فعالی نظیر سدیم ، پتاسیم و منیزیم قرار نگیرد. از نگهداری این ترکیب در مجاورت موادی که با این ترکیب گاز سمی (مانند سدیم سیانید و سولفید آهن) تولید میکنند، اجتناب کنید. از نگهداری جامدات یا اسیدهای اکسید کننده در مجاورت این اسید خودداری کنید. این ماده باید از نقره، کلرید و اوره نیز دور نگه داشته شود زیرا با این مواد ناسازگار میباشد.
دلیل و نحوه استفاده از اسید فرمیک و اسید اگزالیک در صنعت زنبورداری

اسید اگزالیک در سال 2015 برای استفاده در کندوهای زنبور عسل تاییدیه گرفت. به این علت که این ماده یک درمان مستقیم و موثر برای کنههای واروآ محسوب میشود. مخصوصا در اروپا و کانادا طرفداران بسیاری داشته و توسط زنبور داران به طور گستردهای استفاده میشود. طبق نظریات مختلف، این ماده از طریق پاهای زنبور وارد شده، سپس به طرف جریان خون آن حرکت کرده و بیماری را از این طریق از بین میبرد. به هر حال استفاده بیرویه از هر مادهای خطرناک و آسیب زننده است. هنگام استفاده از اسید اگزالیک، نکات ایمنی را جدی بگیرید و مقدار آن را نیز رعایت کنید. از آن جایی که اسید اگزالیک قیمت مقرون به صرفهای دارد و مادهای طبیعی است، در نهایت استفاده از آن نیز برای عموم زنبور داران ممکن است.
در ادامه بررسی کاربرد و اهمیت اسید فرمیک و اسید اگزالیک در صنعت زنبورداری، لازم است بار دیگر به کنههای واروآ اشاره کنیم. این کنهها با هدف کشتن زنبورها وارد کندو شده و خلاصی از آن ها اصلا آسان نیست. به همین منظور اسید فرمیک به کمک زنبور داران آمده و درست مانند اسید اگزالیک عمل خواهد کرد. این ماده مقاوم است، اما در هوای گرم اتاق، تبخیر شده و طبق گزارشها و تحقیقات، بخار آن موجب از بین رفتن کنههای واروآ میشود.
نحوه استفاده از این ماده در کندوها بسیار ساده است. محصولاتی در کشور کانادا تولید شدهاند که حاوی پنبههای آغشته به اسید فرمیک هستند. با قرار دادن آنها در کندو، موجب جذب بخار آب موجود در فضا و آزاد کردن بخار اسید فرمیک میشود. با آزاد شدن آرام و به تدریج این بخار، تمام کنهها از بین رفته و شاهد بهترین نتیجه خواهید بود. از آن جایی که هیچ درمان صد در صدی برای درمان کنههای واروآ موجود نیست، اسید فرمیک نیز دارای مشکلاتی است که زنبور داران باید به آن توجه کنند:
- دمای نامناسب در تبخیر: توجه به دمای هوا در حین استفاده از اسید فرمیک بسیار ضروری است تا در فرآیند بخار شدن این ماده اختلالی ایجاد نشود.
- کشته شدن تعدادی از زنبورها: ممکن است برخی از زنبورها را در این فرآیند از دست بدهید. زیرا هر درمانی، تعداد کمی تلفات را دارد و جای نگرانی نیست. از آنجایی که اسید فرمیک در زنبور ها استرس ایجاد میکند، تعداد کمی از آنها که در حال حاضر ضعیف هستند، ممکن است قربانی این استرس شده و از بین بروند.
- تغییر ملکه: این مورد بسیار نادر است. اما به هر حال ممکن است، زنبور ها ملکه خود را تغییر دهند و این تغییرات در تولید عسل تاثیر بگذارد.
سیکل زمانی استفاده از این محصول در زنبورداری

سیکل استفاده از این ماده برمیگردد به فصول زمانی تولیدمثل زنبورها، طبق بررسیها استفاده از این ماده سالی دوبار (یک بار در اواخر تابستان و بار دوم با شروع زمستان) انجام میشود.
سوالات متداول
-
اثرات اسید اگزالیک بر بدن انسان چیست؟
استفاده و مصرف بیش از حد مواد غذایی حاوی اسید اگزالیک منجر به ایجاد سنگ کلیه میشود. این ماده از جذب کلسیم و آهن به علت خاصیت کیلیت کنندگی ای که دارد جلوگیری میکند. در صورت مصرف بالای مواد غذایی حاوی آن منجر به فقر آهن و مشکلات استخوان شود.
-
اسید فرمیک در چه غلظتی قابل اشتعال است؟
اسید فرمیک در غلظت 85٪ قابل اشتعال است. اسید فرمیک خالص مایعی است که نقطه اشتعال آن 69+ درجه سانتیگراد است، که بسیار بالاتر از میزان بنزین (40- درجه سانتیگراد) یا اتانول (13+ درجه سانتیگراد) میباشد.
نتیجهگیری
اگر با کنه واروآ رو به رو شدید، لازم است مطالبی مرتبط با کاربرد و اهمیت اسید فرمیک و اسید اگزالیک در صنعت زنبورداری را مطالعه کنید، زیرا این دو ماده به از بین رفتن کنهها کمک شایانی کرده و در صورت مراقبت، به عسل و تعداد زنبور هایتان کمترین آسیب را خواهند رساند.